界面新闻记者 |
界面新闻编辑 | 谢欣
此前“停工停产”、备受关注的阿尔茨海默病国产1类新药甘露特钠胶囊(GV-971,商品名:九期一)获得新归宿。
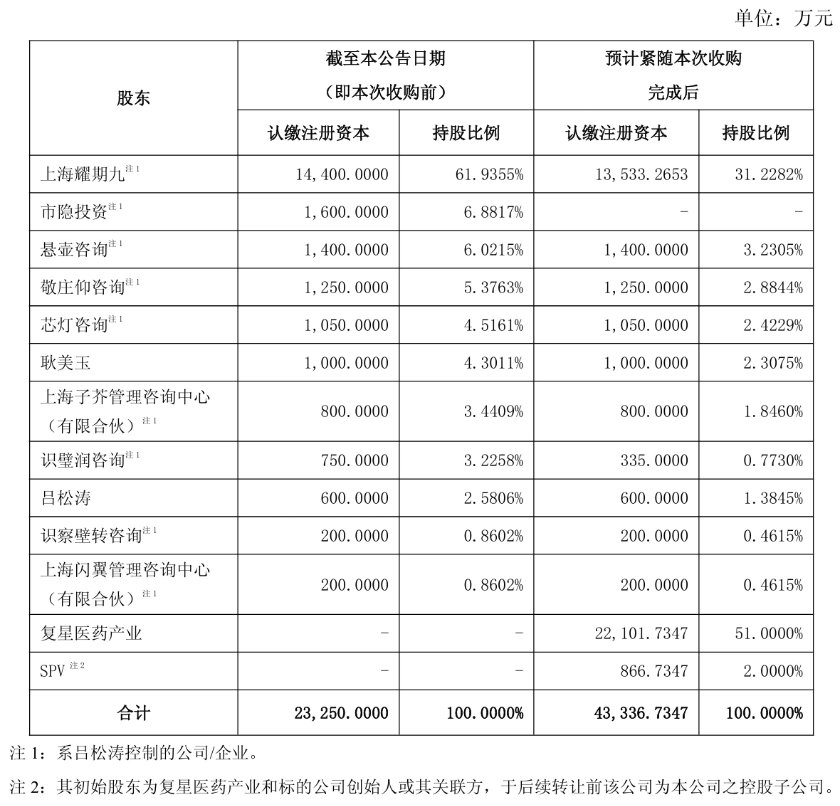
12月15日盘后,复星医药发布公告称,拟以14.12亿元控股甘露特钠胶囊持有方绿谷医药。交易完成后,复星医药将通过复星医药产业及SPV (Special Purpose Vehicle,特殊目的实体)合计持有绿谷医药53%股权,后者将被并表进复星医药。
12月16日开盘,复星医药股价则一路走低,截至上午收盘报26.76元/股,跌4.19%,当下市值714.6亿元。
虽然阿尔茨海默病患者人群多、市场空间巨大,但甘露特钠胶囊和绿谷医药亦不乏争议。对于该收购,业内直呼“看不懂”。一位创新药领域资深投资人亦告诉界面新闻“不完全理解”。

复星医药在本次公告中给出的出手理由则包括进一步丰富其中枢神经系统治疗领域的创新产品管线矩阵,打造诊疗一体、多技术路径协同的解决方案。此前,其已布局脑磁图仪、磁波刀等非侵入式诊疗设备平台、许可引进在研小分子口服药物AR1001(拟用于延缓阿尔茨海默病疾病进程)等。
甘露特钠胶囊是绿谷医药核心且目前唯一的产品。该药是一种以海洋褐藻提取物为原料,制备获得的低分子酸性寡糖化合物,由上海药物研究所、中国海洋大学、绿谷医药联合开发。
2019年11月,该药获国家药监局(NMPA)附条件批准上市,用于轻度至中度阿尔茨海默病,改善患者认知功能,成为首款中国原创、国际首个靶向脑-肠轴的阿尔茨海默病治疗新药。不过NMPA同时要求其上市后继续进行药理机制方面的研究和长期安全性有效性研究,完善寡糖的分析方法,按时提交有关试验数据。
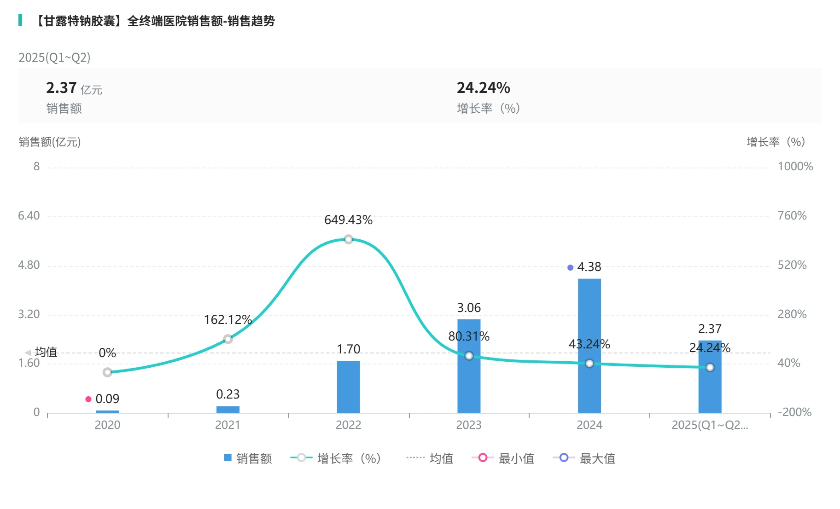
2021年12月,甘露特钠胶囊进入国家医保目录。界面新闻在摩熵·医药数据库检索到,以全终端医院销售额计,其2023年、2024年销售额分别为3.06亿元、4.38亿元。
不过复星医药当下拿到手的并非一款直接能商业化销售的产品。
由于原注册批件到期,新注册证迟迟未获批,2024年11月起,甘露特钠胶囊未再开展商业化生产。到2025年年中,绿谷医药还被曝出资金困难、裁员。
复星医药亦在本次公告中表示,完成收购后将持续有序推进甘露特钠胶囊的上市后确证性临床试验,以使该药尽快获得国家药品审评部门批准。另外此后还需要重新申请医保准入。换而言之,复星医药接盘起码使该药研究得以继续。
而实际上,甘露特钠胶囊获批以来始终毁誉参半。
一方面,该药一路由“重大新药创制”国家科技重大专项等多个重磅项目支持。且其上市前,已十余年未有阿尔茨海默病新药获批,也就是说该药上市能满足一定的临床需求。12月16日,复星医药告诉界面新闻,甘露特钠胶囊上市以来累计惠及患者数十万人,最长患者使用时长6年。
但另一方面,阿尔茨海默病病因复杂、机制未明。甘露特钠胶囊在作用机制、临床设计、研究数据多方面都受到业内挑战。如业内认为其国内三期临床仅在主要终点ADAS-cog量表上有效,指标单一且有主观性;试验持续仅9个月(36周)时间过短等。
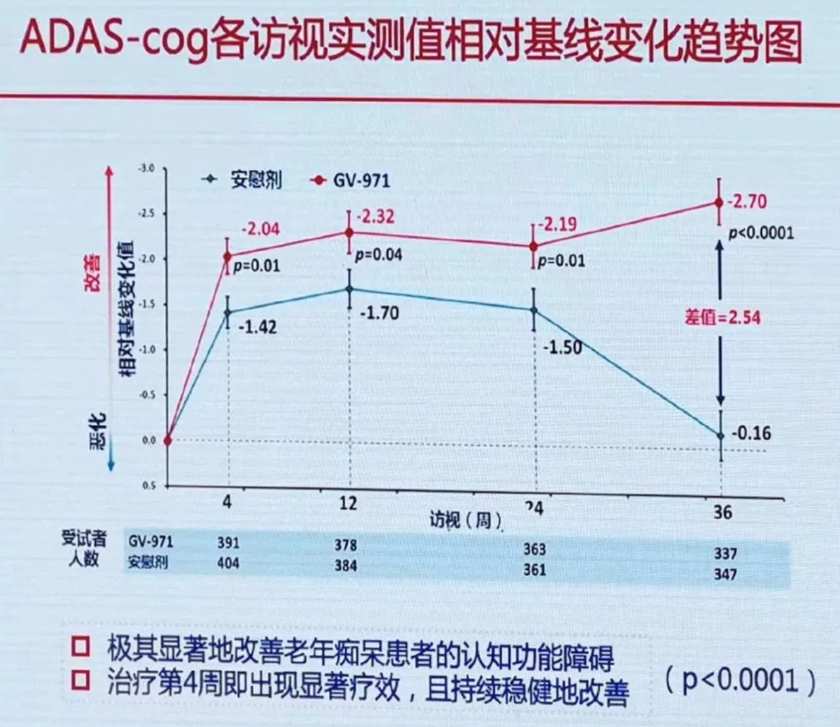
原首都医科大学校长饶毅就多次质疑该药发明人耿美玉研究员学术造假。一张甘露特钠胶囊的ADAS-cog各访视实测值相对基线变化趋势图也广为流传,当中最后12周安慰剂组指标突然大幅恶化,并与试验组拉开差距,令业内人士不解。
针对关于该药的质疑,12月16日,复星医药向界面新闻表示,从目前已开展的国内临床数据来看,无论是单药治疗,还是联合/序贯治疗,甘露特钠胶囊都能让患者获益,主要特点是具备“缓解症状和改变病程进展”的双重潜力,且安全性与治疗依从性较好。
此外,甘露特钠胶囊获批后,绿谷医药不仅在国内开展了上市后长期疗效和安全、长期安全性两项研究,亦曾展开过一项国际多中心三期临床,来验证其临床价值。不过该研究于2022年5月受新冠疫情、公司资金等影响而被终止。复星医药亦在本次公告中称将适时重启该药的国际多中心研究。
而值得一提的是,即使甘露特钠胶囊重新获批、再度归来,其面临的已不是“十几年来的治疗空白”。
界面新闻注意到,12月7日国家医保局公布的首版商保创新药目录中,卫材/渤健的仑卡奈单抗、礼来的多奈单抗位列其中。这两个进口产品均用于治疗由阿尔茨海默病引起的轻度认知障碍和阿尔茨海默病轻度痴呆,均为抗β淀粉样蛋白(Aβ)免疫治疗药物,属于对因治疗药物。
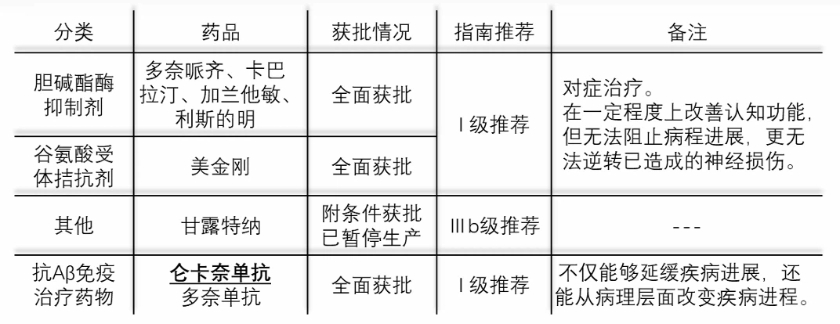
位列商保创新药目录也意味着,这两款阿尔茨海默病新药被国家医保局认可创新程度高、临床价值大、患者获益显著,且在未来放量上具有一定优势。
